

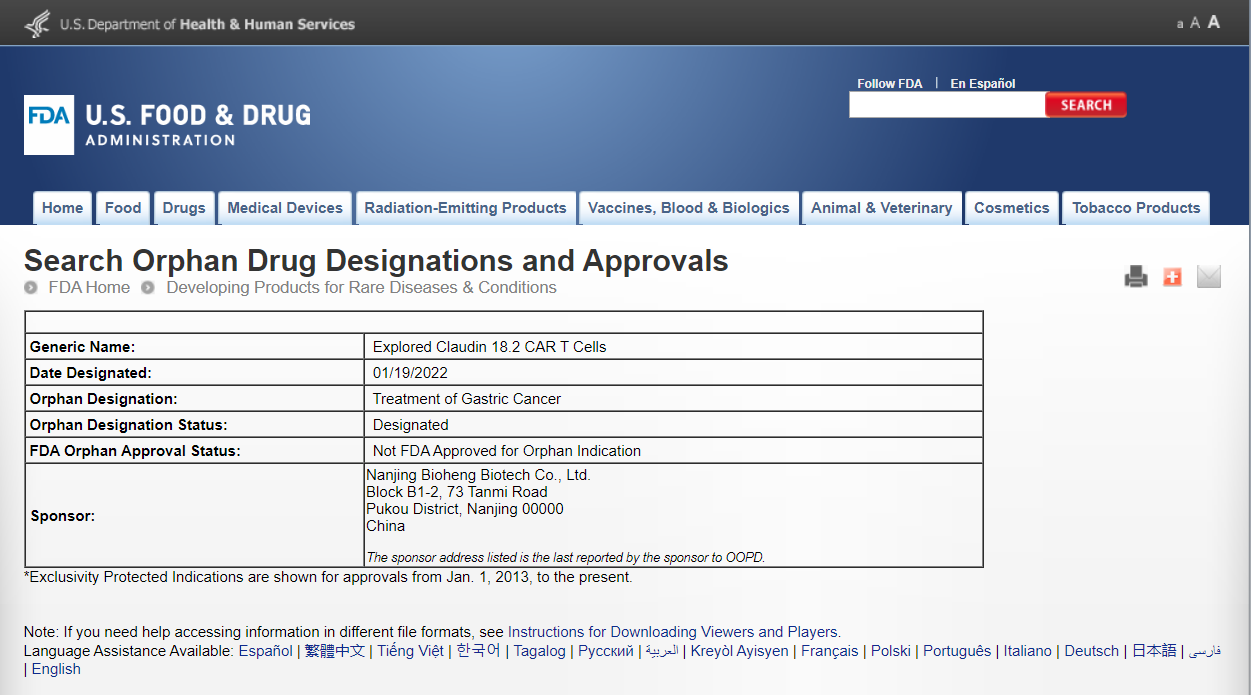
(圖源:FDA官網)
關于CTB001 :
Claudin18.2 是一種泛癌靶點,在各種原發性腫瘤和轉移灶中異常表達,包括胃癌、胰腺癌、膽管癌、卵巢癌和肺腺癌等。CTB001是一種靶向claudin18.2的第四代自體CAR-T細胞治療產品,采用北恒生物Explored CAR-T平臺技術,增強產品的抗腫瘤療效。
CAR-T療法的突破為腫瘤治療提供了新的解決方案,存在著極高的未滿足的臨床需求,CTB001更是在探索性臨床研究中展示出了優異的療效和卓越的安全性,為即將到來的國內申報提供了強有力的數據支持。
北恒生物表示:
CTB001是北恒生物自有Explored CAR-T平臺技術首次進行臨床驗證,是一種非常有前景的,能夠精準、快速、高效給claudin18.2陽性的癌癥患者帶來良好獲益的免疫治療方法。
此次 CTB001獲得FDA孤兒藥資格認定,將進一步加快細胞與基因治療的研發和商業化進程,同時推動北恒生物進軍全球創新藥市場的布局。未來,我們期待將更多的產品推向臨床,為解決未滿足的醫療需求提供更多選擇。
關于孤兒藥:
孤兒藥是指用于預防、治療、診斷罕見病的藥品。而罕見病是一類發病率極低的疾病,在美國罕見病是指患病人群少于20萬的疾病。在研藥物獲得ODD后,制藥公司可以獲得各種藥物開發激勵措施,包括在美國進行臨床研究產生的費用可獲得25%的聯邦稅收抵免;免除《處方藥使用者付費法案》(The PrescriptionDrug User Fee Act, PDUFA)的費用;競爭獲得孤兒產品開發辦公室(Office of Orphan Products Development,OOPD)的研究資助,以支持孤兒藥的臨床研究;獲得FDA的監管指導,設計總體的藥物開發計劃;藥品的7年市場獨占權。
關于北恒:
南京北恒生物科技有限公司(以下簡稱“北恒生物”)成立于2017年,是一家專注于疾病治療產品開發及商業化的創新型生物醫藥公司,由國內外頂尖學府的博士及經驗豐富的運營團隊聯合創立,業務涵蓋免疫細胞和基因治療等領域。北恒生物現擁有7500㎡高標準臨床轉化中心及GMP生產車間,涵蓋質粒病毒生產、細胞擴增及質控等,符合FDA及NMPA對細胞治療制品監管的嚴格標準。
2021年3月北恒生物獲得高瓴創投、德誠資本和八方資本等領投的5.2億元B輪投資,目前累計完成融資近7億元。截至2021年11月,公司已申請核心專利52件,入選“培育獨角獸企業”、“哪吒企業”、江蘇省“雙創人才”計劃、南京市高層次創業人才引進計劃、南京市專家工作室等; 已獲得國家科技型中小企業、知識產權管理體系認證企業、南京市工程研發中心等榮譽。
北恒生物開發的第五代“現貨”通用型CAR-T細胞治療產品,具有國際領先的研發水平,有望從根本上解決當前CAR-T治療“成本高、時間久、生產難、個性化”的困境,實現免疫細胞治療的可負擔性和可及性。北恒生物一直秉承“求索、創新、務實、高質”的核心價值觀拼搏進取、勇于創新,立做世界領先的生物醫藥創新型公司,搭建生命與健康之橋,讓每一位患者得到治愈機會。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn