


近日,蘭州大學藥學院劉映前教授團隊與華中科技大學同濟藥學院徐傳瑞教授團隊合作,在抗腫瘤新藥發現與腫瘤治療方面取得新進展。相關研究成果“Design and synthesis of Aza-boeravinone derivatives as potential novel topoisomerase I inhibitors”發表于Bioorganic Chemistry期刊(IF:5.275)上。蘭州大學藥學院2020級碩士研究生周勇和2019級碩士研究生白銀鵬為該論文共同第一作者,通訊作者為劉映前教授和徐傳瑞教授,蘭州大學藥學院為該論文的第一單位。
腫瘤是世界上大多數國家的主要死亡原因之一。根據世界衛生組織(WHO)統計,2020年全球估計有1930萬新病例的產生和1000萬腫瘤病例的死亡,并且全球腫瘤的發病率和死亡率正在迅速增加。因此,研究和開發新的藥物和治療策略以控制腫瘤顯得尤為迫切和重要。其中,化療在腫瘤的治療中仍然扮演著舉足輕重的作用。DNA拓撲異構酶I(Top I)抑制劑是抗腫瘤藥物的重要組成部分,在晚期實體瘤和女性癌癥中發揮著越來越重要的作用。Top I是真核生物中必需的酶,參與細胞DNA復制、轉錄、重組和染色體分離等眾多過程。多項研究表明,與正常細胞相比,Top I在腫瘤細胞中高度表達并且促進腫瘤生長。因此,Top I已經被證明是抗腫瘤的重要靶點之一。
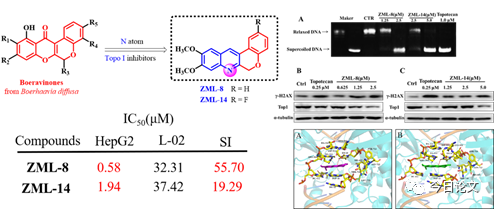
藏藥喜馬拉雅紫茉莉為紫茉莉科植物喜馬拉雅紫茉莉(Mirabilis himalaica (Edgew.) Heim.)的干燥根。Boeravinones是從喜馬拉雅紫茉莉中分離得到的一類天然產物,具有廣泛的生物學活性,如抗炎、抗菌、抗氧化、抗病毒和抗腫瘤等。但其自身抗腫瘤譜窄且活性較弱,需進一步進行結構優化或改造而增強活性。因此,基于天然產物Boeravinones的結構骨架,該研究團隊采用生物電子等排和“Aza”結構優化策略設計合成了兩個系列的6H-色烯并[3,4-b]喹啉衍生物。
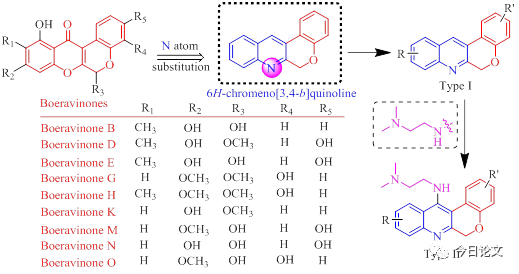
Figure 1. Structures of boeravinones from Boerhaavia diffusa and novel structures of 6H-chromeno[3,4-b]quinoline derivatives.
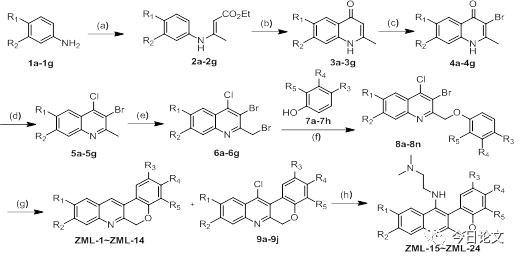
Figure 2. Reagents and conditions: (a) ethyl acetoacetate, AcOH, benzene,reflux; (b) Ph2O, 250 ℃; (c) NBS, AcOH/DCM(1:2), rt; (d) POCl3, reflux; (e)benzoyl peroxide, NBS, CCl4, reflux; (f) NaH, DMF, rt; (g) Pd(OAc)2, PPh3,K2CO3, DMF, 120 ℃; (h) N,N-Dimethylethylenediamine, pridine, 120℃.
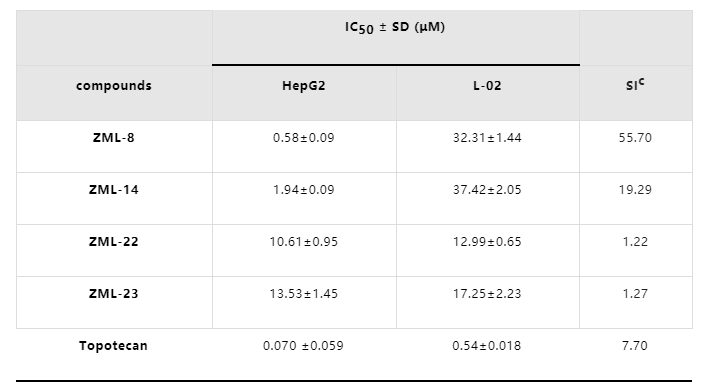
作者首先評估了所得化合物對HepG2、A2780、Hela、HCT116、SW1990和MCF7等多種腫瘤細胞株的細胞毒活性。篩選結果發現,化合物ZML-8和ZML-14對HepG2具有顯著的抑制效果,IC50值分別為0.58μM和1.94 μM。此外,化合物ZML-8和 ZML-14對HepG2 和 L-02 細胞的選擇性高于對照藥Topotecan。因此,進一步研究了候選化合物ZML-8和ZML-14的抗腫瘤效果與作用機制。
Table 1. Antiproliferative Activities of Compounds ZML-8, ZML-14, ZML-22, and ZML-23 against Normal Human Liver Cell Line L-02.
通過流式細胞術、Western blotting等實驗研究表明,化合物ZML-8 和ZML-14劑量依賴性地誘導HepG2細胞周期G2/M期阻滯。此外,化合物ZML-8和 ZML-14誘導HepG2細胞凋亡并伴隨促凋亡蛋白Bax、Bad和Cleaved-caspase3的激活以及抗凋亡蛋白Bcl-2的降低。這些結果表明,化合物ZML-8和 ZML-14誘導Caspase依賴的細胞凋亡。
Figure 4. Compounds ZML-8 and ZML-14 caused G2/M cell cycle arrest of HepG2 cells. (A)Cell cycle distribution HepG2 cells treated with compound ZML-8 and ZML-14 for24 h, Topotecan was used as positive control. Treated cells were then stained with PI/RNase and analyzed using a flow cytometer. (B) Sums of percentages of each cycle were shown as mean ± S.D. for three independent experiments (*P <0.05, **P < 0.01, ***P < 0.001.vs. the control).
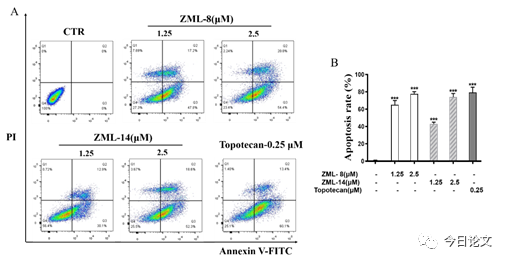
Figure 5. Compounds ZML-8 and ZML-14 induced apoptosis of HepG2 cells. (A) Apoptosis in HepG2 cells treated with compound ZML-8 or ZML-14. Cells were exposed to compound ZML-8, ZML-14, or Topotecan for 48 h. The apoptosis rates were then assessed by Annexin V/PI double staining determined by flow cytometry. (B) Apoptosis rates were shown onthe histogram for three independent experiments. Data were shown as mean ± SD.*P < 0.05 or **P < 0.01 or ***P < 0.001 vs. the control.
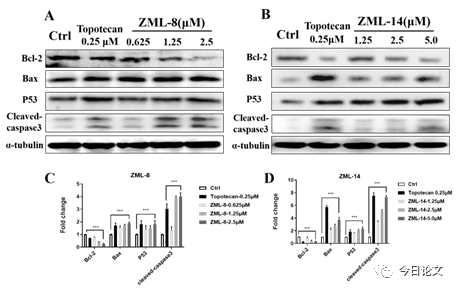
Figure 6. Western blotting analysis of Caspase-dependent apoptosis proteins in HepG2 cells after compounds ZML-8 and ZML-14 treatment. HepG2 cells were treated with compound ZML-8, ZML-14, or Topotecan for 48 h. The cells were harvested and lysed to detect cleaved Caspase-3, P-53 and Bcl-2 members (Bcl-2 and Bax) using Western blot. α-Tubulin was used as reference. (A) and (B) Representative western blots of proteins in compound ZML-8 or ZML-14 treated cells. (C) and (D) Quantification of western blot. Results are representative of three independent experiments. *p < 0.05,**p < 0.01, and ***p < 0.001 vs control.
根據上述實驗結果,化合物ZML-8和ZML-14通過誘導細胞周期阻滯和細胞凋亡來抑制細胞增殖,并且該結果與對照藥物Topotecan相似。為此,作者假設化合物ZML-8 和 ZML-14 可能具有與Topotecan相似的作用機制。DNA松弛實驗結果表明,化合物ZML-8 和 ZML-14顯著抑制Top I的酶活性。化合物ZML-8和ZML-14分別在2.5 μM 和5.0 μM濃度劑量下具有與1.0 μM的 Topotecan抑制效果。此外,Western blotting結果表明,化合物ZML-8 和 ZML-14誘導Top I蛋白水平降解。據報道,抑制 Top I 或捕獲 Top1cc 可導致 DNA 損傷。因此,作者進一步檢測了DNA損傷的生物標志物γ-H2AX的表達情況。研究發現,化合物ZML-18和ZMl-14處理后γ-H2AX的蛋白表達水平顯著增加,表明誘導了DNA損傷。分子對接結果進一步表明,化合物ZML-8和ZML-14可以與Top I-DNA 復合物相互作用,結合能分別為-9.4 kcal/mol和-9.7kcal/mol。
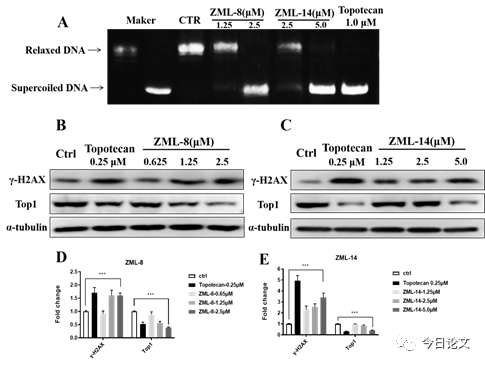
Figure 7. Compounds ZML-8 and ZML-14 down-regulated the Top1 activity and induced DNA damage. (A) The inhibitory activity of compounds ZML-8 and ZML-14 on Top1. Lane 1: relaxed DNA; Lane 2: supercoiled plasmid DNA (pBR322) only; Lane 3: DNA + Top1+DMSO; Lane 4-5: DNA + Top1+ ZML-8; Lane 6-7: DNA + Top1+ ZML-14; Lane 8: DNA + Top1+ Topotecan,were used as positive control. (B) and (C) HepG2 cells were treated with compounds ZML-8 and ZML-14 for 48 h, harvested and lysed for detection of Top1 and γ-H2AX. (D) and (E) Histograms of relative expression of Top1 and γ-H2AX. Data are shown as mean ± SD of three independent experiments. *p < 0.05, **p < 0.01, and ***p < 0.001 vs control.
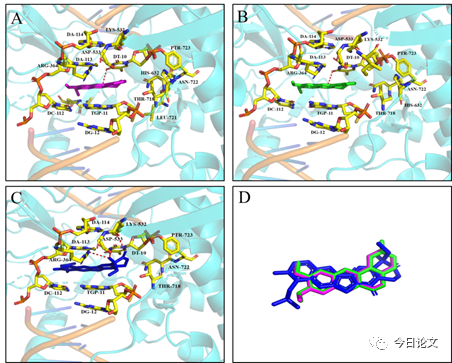
Figure 8. Hypothetical binding mode of compounds ZML-8 and ZML-14 in the ternary Top1-DNA-drug complex (PDB ID: 1K4T). Protein is shown as a cartoon, and compounds ZML-8, ZML-14 and Topotecan were shown in stick. Key hydrogen-bonding interactions are indicated with yellow dashes. (A-C) Compounds ZML-8 (pink), ZML-14 (green) and Topotecan (blue) were shown in the ternary complex with a docking energy -9.40, -9.70 and -12.4 kcal/mol, respectively.(D) Overlapping of the binding pose of compounds ZML-8 (pink) and ZML-14(green) with Topotecan (blue).
綜上,基于天然產物Boeravinones的結構骨架,團隊采用生物電子等排策略設計合成了兩個系列的6H-色烯并[3,4-b]喹啉衍生物,并評估了所得化合物對HepG2、A2780、Hela、HCT116、SW1990和MCF7等腫瘤細胞株的細胞毒活性。篩選結果表明,化合物ZML-8和ZML-14對HepG2具有顯著的抑制效果,IC50值分別為0.58μM和1.94 μM。此外,化合物ZML-8和ZML-14對HepG2和L-02細胞的選擇性高于對照藥Topotecan。細胞機制研究表明,化合物ZML-8和ZML-14誘導HepG2細胞周期G2/M期阻滯、細胞凋亡和DNA損傷。此外,化合物ZML-8和ZML-14顯著抑制Top I的酶活性,并且誘導Top I蛋白水平的降解。分子對接表明,化合物ZML-8和 ZML-14顯著的細胞毒活性是由于與Top1-DNA復合物的良好相互作用。
這項研究的重要進展為后續開發具有完整自主知識產權的抗腫瘤藥物奠定了基礎。課題組長期致力于天然源抗腫瘤藥物的設計合成與創制研究,為臨床抗腫瘤藥物的開發提供科學依據。研究工作得到了浙江省重點大學優勢特色學科開放項目、甘肅省國際科技合作重點項目和國家自然科學基金共同資助。該項研究也是依托甘肅省中藏藥功效物質開發與利用行業技術中心,開展源于天然源藏藥資源進行新藥開發研究取得的又一重要的科研成果,對于推動中藏藥功效物質開發與利用具有重要意義。
原文鏈接:https://doi.org/10.1016/j.bioorg.2022.105747
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn