

自2019年底以來,嚴重急性呼吸系統綜合征冠狀病毒2 (SARS-CoV-2)已經在全世界范圍內引起了約5.3億人感染,導致約1800萬人死亡。幾乎所有感染SARS-CoV-2的死亡患者都被發現是有細胞因子風暴綜合癥和病毒敗血癥,過度的炎癥反應導致死亡率的增加,因此,防止過度炎癥是避免細胞因子風暴綜合癥的關鍵。然而,目前,在臨床或研究中應用的抗炎藥物或免疫調節劑,包括針對炎癥細胞因子(sarilumab, anakinra, tocilizumab,infliximab, adalimumab)及炎癥途徑(baricitinib, ruxolitinib)等藥物,均易引發二次感染加重疾病的進程,因此,目前尚無針對性的特效抗SARS-CoV-2炎癥的藥物,尤其是缺少安全性和高選擇性的抗炎藥物。

近日,四川大學生命科學學院宋旭教授/趙永云課題組在國際權威期刊Signal Transduction and Targeted Therapy(IF=18.187)發表題為Aptamer Blocking S-TLR4 Interaction Selectively Inhibits SARS-CoV-2 Induced Inflammation的文章,篩選和鑒定了可抑制SARS-CoV-2誘發的炎癥的核酸適配體,該核酸適配體通過特異性阻斷Spike蛋白與TLR4受體相互作用,高選擇性地抑制SARS-CoV-2病毒所誘發的炎癥。
該研究通過Beads-Based SELEX法篩選Spike的核酸適配體,為確保高親和力、特異性及穩定性的進化效率,在篩選過程中,通過正篩、負篩和加壓篩選的方式,篩選了一系列富含G的核酸適配體作為候選序列,并對序列進行了一系列的截短優化,通過評價核酸適配體的親和力、穩定性、特異性、動物免疫源性,最終獲得3條含有G-四聚體結構、高親和力(KD = 30-80 nM)及高特異性的阻斷Spike蛋白與TLR4受體相互作用的核酸適配體 (ST-6、ST-6-1、ST-6-2),在血清和小鼠體內均顯示具有良好的穩定性,且免疫源性低的優點,說明具有良好的成藥潛能。
對核酸適配體抑制SARS-CoV-2誘發炎癥的能力進行評估,結果顯示這3條DNA適配體對分別模擬的預防期、及感染窗口期、治療期均具有顯著的抗炎能力,并且,對SARS-CoV-2的突變株如Lambda,Delta,Omicorn的Spike所引發的炎癥反應依然具有顯著的抑制效果。對真實的SARS-CoV-2病毒誘發的炎癥(IL-1β,IL-6,TNF-α,IFN-β,IL-8)的抑制能力約為75%,表現出很好的治療炎癥的潛能。
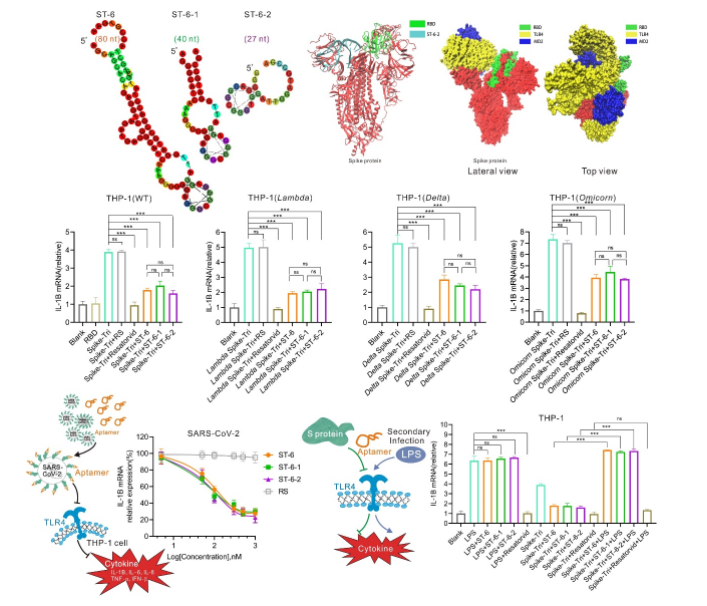
設計抗炎藥的一個主要挑戰是平衡功效和安全性,特別是確保其不會損害宿主對其他細菌或病毒感染的防御能力。因此,對這些核酸適配體是否損害宿主的免疫功能進行了評估。結果顯示采用Spike和核酸適配體預處理的細胞,依然可以在LPS刺激下產生正常的免疫反應,說明這3條DNA適配體不會損害宿主的免疫功能而引發二次感染,是高選擇性的抗SARS-CoV-2炎癥的抑制劑。綜上,將這些抗病毒炎癥的核酸適配體與抗病毒感染的藥物進行聯合使用是有效治療SARS-CoV-2的潛在藥物。
該項目得到了廣州醫科大學P3實驗室的趙金存教授的大力支持,四川大學生命學院2019級碩士生楊港、廣州醫科大學博士后張勝男、四川大學生命科學學院2020級碩士生王玉春、李靈副研究員為論文第一作者,四川大學生命科學學院趙永云特聘副研究員、宋旭教授和廣州醫科大學趙金存教授為共同通訊作者。該研究獲得了國家重點研發計劃、成都市科技創新項目等經費的支持。相應的核酸適配體已申報國家發明專利(申請號:2021114447608)。
原文鏈接:https://doi.org/10.1038/s41392-022-00968-2
參考資料:https://life.scu.edu.cn/info/1095/4051.htm
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn